Olá pessoal,
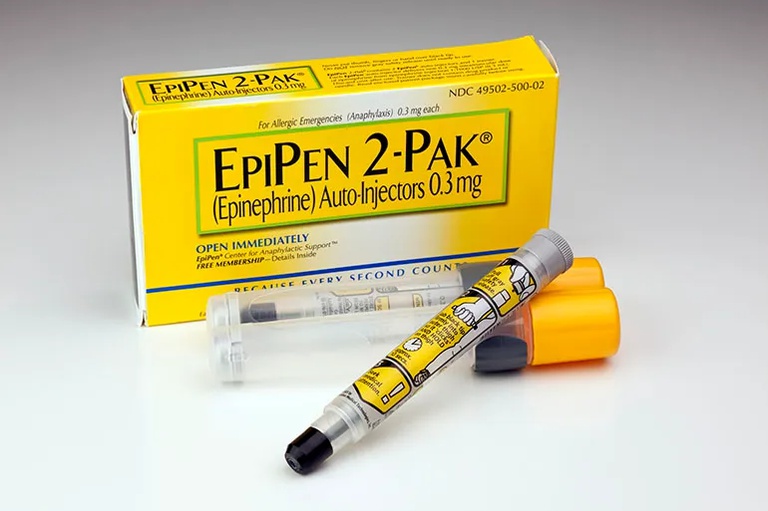
Recentemente conversei com a mãe de uma criança com asma grave que passa um perrengue sempre que precisa renovar o estoque de EpiPen (caneta injetável de adrenalina), então resolvi aprofundar nesse assunto.
A Anvisa proibiu o uso de comercialização, mas como ficam os pacientes?
O medicamento é seguro e tem liberação do FDA gente… 👀 .
Boa leitura!
Tempo de leitura : 5 minutos
💬 Em pauta
Quando uma mãe me falou: “Doutor, é sempre um perregue, porque preciso importar ou pedir para algum conhecido trazer dos EUA”, fiquei pensando…
Por que não temos EpiPen no Brasil? Algo travado na ANVISA, falta de vontade da farma?
O EpiPen é indicado para o tratamento de emergência da anafilaxia em crianças, independentemente do gatilho. Os principais desencadeantes incluem alimentos (amendoim, castanhas, leite, ovo, frutos do mar), picadas de himenópteros, medicamentos, látex, imunoterapia e formas idiopáticas ou induzidas por exercício.
A prescrição profilática está indicada em:
Episódio prévio de anafilaxia
Alergia alimentar IgE-mediada com fatores de risco (asma concomitante, alergia a amendoim ou frutos do mar)
Reação sistêmica a veneno de himenóptero
Mastocitose ou triptase basal elevada
Acesso difícil a serviços de emergência
A posologia segue o peso: EpiPen Jr 0,15 mg para crianças de 7,5 a 25 kg e EpiPen 0,30 mg acima de 25 kg, sempre via intramuscular na face anterolateral da coxa, podendo ser repetido em 5 a 15 minutos se a resposta for inadequada. No Brasil, dada a disponibilidade irregular do dispositivo, a ASBAI orienta alternativas com ampolas de adrenalina 1 mg/mL.

Mas olha o tamanho do problema!
Em 2024, foram registrados 1.143 internações por anafilaxia no país (ainda subestimado na minha opinião), um aumento de 107% em comparação a 2015.

A caneta de adrenalina tem eficácia comprovada para casos graves de alergia, mas, apesar de ser usada há décadas no exterior, ela não está disponível no Brasil.
O EpiPen é um recurso prático e eficiente contra a anafilaxia, mas ainda não há interesse por parte das fabricantes em comercializar o produto no país 🫠 , apesar das demandas de associações médicas brasileiras e do aumento de casos e fatalidades na última década.
A Anvisa tem melhorado bastante o seu SLA para avaliação e liberação de novos medicamentos (quando comparamos com a última década), mas também tem demonstrado uma falta de pró-atividade para liberar medicamentos de interesse público.
Lembra dessa da época no Metanol? 👇 Não tínhamos o medicamento que reverte a intoxicação (Fomepizol) e nem liberação, ai tiveram que sair correndo para importar. A tragédia poderia ter sido bem pior.

Hoje, no Brasil, a situação prática é esta:
1. EpiPen/autoinjetor de adrenalina não é comercializado regularmente no Brasil.
A Anvisa registrou em 2025 que não havia registro válido para adrenalina/epinefrina em dispositivo autoinjetável no país, nem pedido de registro em análise naquele momento.
Sem registro sanitário, o produto não pode ser fabricado ou comercializado no Brasil.
2. A venda de EpiPen sem registro é proibida.
Em abril de 2026, a Anvisa determinou a apreensão do autoinjetor de adrenalina EpiPen importado pela Farmácia Pague Menos e proibiu armazenamento, comercialização, distribuição, propaganda e transporte do produto sem registro no Brasil.
3. O que existe no Brasil é adrenalina injetável em ampola.
A Anvisa informa que há medicamentos com registro ativo contendo adrenalina/epinefrina em solução injetável 1 mg/mL, em ampolas de 1 mL, com vias IM, IV e SC. Entre as indicações aprovadas estão anafilaxia e choque anafilático.
4. Para ter autoinjetor, o caminho atual costuma ser importação para uso pessoal.
A ASBAI (Associação Brasileira de Alergia e Imunologia) resume que, por ausência de registro na Anvisa, os autoinjetores não são comercializados no Brasil e precisam ser importados. Na prática, isso exige prescrição/laudo médico e atenção às regras sanitárias e aduaneiras.
5. Ainda não há obrigação federal ampla de fornecimento pelo SUS ou de estoque em escolas/lugares públicos.
Existem projetos de lei em tramitação (PL 85/2024). Em julho de 2025, a Comissão de Saúde da Câmara aprovou projeto para incluir adrenalina autoinjetável no SUS e permitir fornecimento em locais com grande circulação, mas a própria Câmara informa que a proposta ainda precisa passar por outras comissões e, para virar lei, ser aprovada pela Câmara e pelo Senado. O negócio está meio parado desde Julho de 2025, pois depende de um ponto VITAL » um laboratório internacional entrar com pedido de registro e importação na ANVISA.

Esse é o cenário atual…
Situação atual (maio/2026):
O PL 85/2024 está "Aguardando Designação de Relator(a) na Comissão de Finanças e Tributação (CFT)". Ou seja, desde o recebimento na CFT em 02/07/2025, o projeto não andou. Depois da CFT, ainda precisa passar pela CCJ. Como tramita em caráter conclusivo (Art. 24, II do RICD), se for aprovado nas duas comissões restantes vai direto ao Senado, sem passar pelo plenário da Câmara.
O que o substitutivo aprovado prevê:
Inclusão da adrenalina autoinjetável na lista de medicamentos do SUS, com fornecimento gratuito mediante laudo médico
Disponibilização também em locais de alto fluxo (≥1.500 pessoas/dia): aeroportos, rodoviárias, shoppings, escolas, templos, etc.
O nó regulatório (que o PL não resolve):
A caneta de adrenalina não tem registro na Anvisa. Em nota recente à Agência Einstein (nov/2025), a Anvisa confirmou que nunca foi protocolado pedido de registro do produto, porque o órgão só pode autorizar registro após solicitação de uma empresa interessada em produzir ou importar o medicamento. Os fabricantes estrangeiros alegam que já atendem mercados maiores e não têm capacidade de expandir produção para o Brasil. Hoje, o acesso é feito por importação individual (custo de R$ 2.000 a R$ 4.000) ou via judicialização, frequentemente com demanda contra a União sob o Tema 1.234 do STF e a Súmula Vinculante 60. Poder360
Movimentos paralelos relevantes:
Grupo da UFRJ (Renato Rozental) desenvolve protótipo nacional, com previsão de chegar ao mercado por volta de R$ 400, dependendo da aprovação Anvisa
PL 884/2024 (Dayany Bittencourt) tramita em paralelo, criando o "Programa Caneta da Vida" para escolas de educação básica, com parecer favorável aprovado na Comissão de Educação
Anvisa fechou acordo de bilateralidade com a FDA, que pode acelerar reconhecimento de dispositivos já aprovados nos EUA
Casos de anafilaxia aumentaram mais de 100% no Brasil em 10 anos, segundo dados da Asbai, com 1.143 episódios em 2024 Poder360
Resumindo a leitura política: o PL é simbolicamente importante e tem apoio das sociedades médicas (Asbai à frente), mas enfrenta um paradoxo prático. Sem registro na Anvisa nem produtor interessado, mesmo se aprovado, o SUS não terá o que distribuir. A solução real depende ou de uma fabricante estrangeira protocolar pedido de registro, ou da viabilização do dispositivo nacional da UFRJ. Por isso, o projeto saiu da Comissão de Saúde quase um ano atrás e perdeu velocidade na CFT, onde costuma encontrar resistência por proposições com impacto orçamentário sem contrapartida clara.
Em resumo…
→ Pode usar adrenalina em anafilaxia? Sim, é tratamento essencial.
→ Dá para comprar EpiPen no Brasil em farmácia? Regularmente, não.
→ Pode vender EpiPen importado? Não. A Anvisa proibiu.
→ Existe autoinjetor registrado no Brasil hoje? Pelas fontes oficiais recentes, não há registro válido.
→ Existe movimento para mudar isso? Sim, há PLs em andamento para SUS, escolas e locais públicos, mas ainda não viraram regra federal ampla.
O que você achou dessa história do EpiPen?
Por hoje é só!
Mandem feedbacks, é só responder esse e-mail.
Se você achou o conteúdo interessante, compartilhe.
Domingo que vem tem mais,
Abraço!
Thiago Liguori